
Кремний — химический элемент IV группы периодической системы Менделеева, атомный номер 14, атомная масса 28,0855. Какими свойствами обладает кремний и каковы его свойства?
Общая химическая характеристика кремния
Кремний — элемент третьего периода группы IVA, p-элемент. В атоме кремния имеется пять вакантных d-орбиталей. При их участии кремний образует соединения, где его координационное число равно 6. Для кремния характерно образование цепочек, в которых чередуются атомы кремния и кислорода, соединенные прочными связями.

Кремний встречается в природе в связанном виде: более половины земной коры состоит из кремнезема SiO2, силикатных алюмосиликатных пород типа каолинита Al2O3*2SiO2*2H2O, основных компонентов песка и глины.
Название этот элемент получил от минерала с латинским названием silisium (silex – означает кремень). Русское название «кремний» введено в 1834 году академиком Г. И. Гессом.
Физические свойства
Известны аморфный и кристаллический кремний. Природа кристаллического кремния такова, что это темно-серое с металлическим блеском тугоплавкое, хрупкое кристаллическое вещество с незначительной проводимостью.
Расположение атомов Si такое же, как у атомов C в алмазе. Каждый атом кремния расположен в центре тетраэдра и ковалентно связан с четырьмя другими атомами кремния. Аморфный кремний представляет собой коричневый порошок, более реакционноспособный.
У кремния в природе встречаются три стабильных изотопа
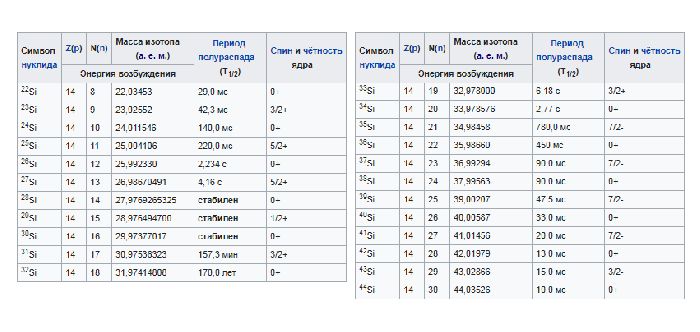
Химические свойства
Поскольку атом кремния имеет четыре электрона на внешнем энергетическом уровне, его характерные степени окисления составляют +4 и -4. Соединения, содержащие кремний со степенью окисления +2, встречаются редко.
В соединениях кремний проявляет IV валентность, при нагревании взаимодействует с простыми веществами (фтором, хлором, кислородом, углеродом).
В обычных условиях кремний из простых веществ реагирует только с фтором:
Реакции с кислородом и фтором протекают при +400-+600 градусов:
Si+2Cl=SiCl4 (тетрахлорид кремния)
Кремний не реагирует с кислотами. С плавиковой кислотой реагирует только аморфный кремний, измельченный в порошок.
Кремний реагирует с горячими растворами щелочей, образуя силикаты и водород:
Кремний химически реагирует со многими металлами с образованием силицидов:
2Mg+Si=Mg2Si (силицид магния)
При действии соляной кислоты на силицид магния Mg2Si образуется силан SiH4:
Силан — бесцветный токсичный газ, аналог метана, самопроизвольно воспламеняющийся на воздухе и горящий с образованием оксида кремния и воды:
Что мы узнали?
В статье описаны физические и химические свойства элемента кремний. Валентность кремния почти всегда IV и лишь в некоторых соединениях появляется валентность II. Кремний при нагревании способен вступать в реакцию с металлами, неметаллами и щелочами.








Комментирование закрыто