
Соединение, находящееся в агрегатном состоянии, занимающее промежуточное положение между твердой и газообразной формой, называется жидким веществом.
Строение
Молекулы в жидкости не имеют строго упорядоченной структуры, как в твердом теле, и могут перепрыгивать из одного места в другое, чем и объясняется течение жидкости. Расстояние между молекулами жидкого вещества близко, но не так велико, как между молекулами газов. Частицы жидкости не отрываются и не движутся свободно и хаотично.
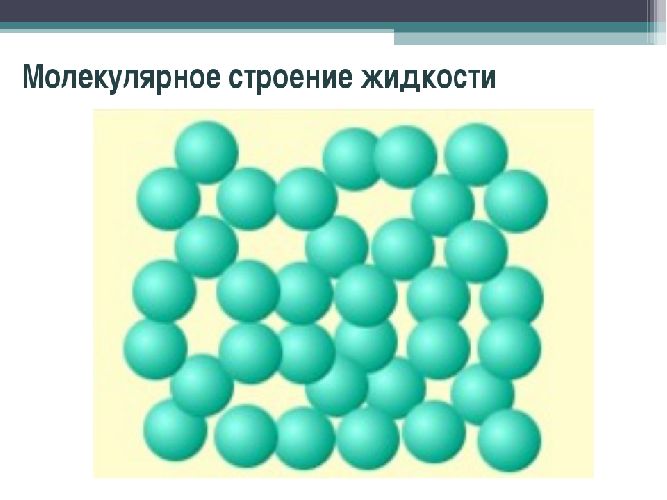
Притяжение между молекулами достаточно сильное, чтобы поддерживать межмолекулярное расстояние, но достаточно слабое, чтобы удерживать молекулы в статическом положении.
Жидкость держит объём, но не держит форму, совершая колебательные движения.
Физические свойства
Жидкости отличаются от газов и твердых тел и обладают индивидуальными свойствами:
- текучесть – способность принимать форму сосуда и двигаться под действием даже небольшой силы;
- вязкость – способность сопротивляться движению одной части вещества относительно другой;
- низкая сжимаемость – невозможность уменьшения объема из-за малого пространства между молекулами;
- смачивание – «приклеивание» молекул жидкости к твердым веществам;
- образование поверхностного натяжения – образование разделения фаз (жидких и газообразных) в виде эластичной мембраны.

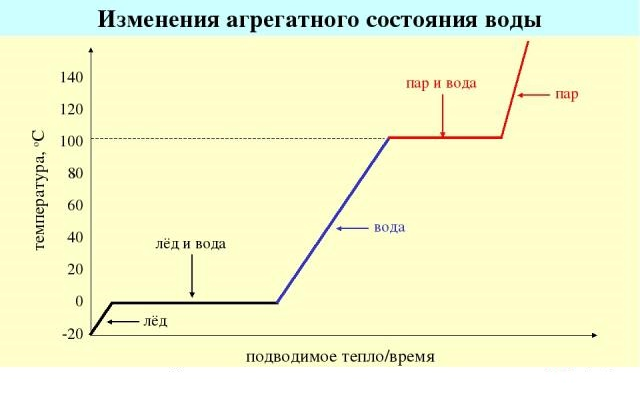
Жидкости могут существовать только в определенном диапазоне температур. При понижении температуры жидкость переходит в твердое состояние, а при повышении температуры — в газообразное вещество. Границы температурного диапазона зависят от давления.
Жидкости условно делят на две группы:
- чистые вещества, состоящие только из молекул;
- смеси, включающие дополнительные частицы и молекулы и другие вещества.
Примерами жидких смесей являются кровь, морская вода и фруктовый сок.
Многие жидкости органического и неорганического происхождения являются растворителями. Это вещества, способные разлагать (растворять) другие жидкие, твердые или газообразные вещества. Растворители включают этанол, спирт, ацетон, воду и аммиак.
В условиях невесомости жидкость приобретает форму капли за счёт поверхностного натяжения, создаваемого со всех сторон.
Классификация
Самая знакомая жидкость на планете – вода. Характеризуется высокой текучестью, замерзает при 0°С, испаряется при 100°С. Вода не обладает высокой вязкостью и является универсальным растворителем.
Однако существует множество других жидкостей, отличающихся от воды по физическим и химическим свойствам. Существуют основные виды:
- атом, состоящий из атомов или сферических молекул (метан, аргон в виде жидкостей);
- двухатомные, состоящие из двух одинаковых атомов вещества (ртути, жидкого водорода, натрия);
- полярные, состоящие из полярных молекул (жидкий бромоводород);
- ассоциированные, в том числе водородные связи (вода, глицерин).
В физике отдельно выделяют квантовые жидкости и жидкие кристаллы.
Что мы узнали?
С 11 класса мы учили, что такое жидкости. Это жидкие вязкие вещества, находящиеся между твердым и газообразным агрегатным состояниями. Жидкость принимает форму сосуда, но при этом имеет свой объем. В жидком состоянии вещества существуют в определенном диапазоне температур. При изменении температуры жидкость превращается в твердое тело или газ. Существует несколько типов жидкостей в зависимости от их химической структуры.








Комментирование закрыто