
Воздух – это смесь газов, необходимая для существования и поддержания жизни на планете. Каковы его свойства и какие вещества входят в состав воздуха?
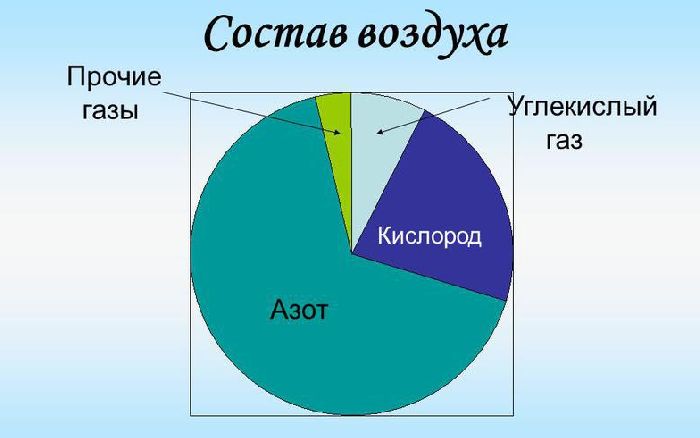
Состав воздуха
Воздух необходим для дыхания всем живым организмам. В его состав входят азот, кислород, аргон, углекислый газ и ряд примесей. Состав атмосферного воздуха может меняться в зависимости от условий и местности. Так, в городской среде уровень углекислого газа в воздухе увеличивается по сравнению с лесной местностью из-за обилия транспортных средств. На больших высотах концентрация кислорода падает, поскольку молекулы азота легче молекул кислорода. Поэтому концентрация кислорода падает быстрее.
Шотландский физик и химик Джозеф Блэк в 1754 году опытным путем доказал, что воздух – это не просто вещество, а именно газовая смесь

Если говорить о процентном составе воздуха, то основным компонентом является азот. Азот занимает 78% от общего объема воздуха. Процент кислорода в молекуле воздуха составляет 20,9%. Азот и кислород — два основных элемента воздуха. Содержание остальных веществ значительно меньше и не превышает 1%. Так, аргон занимает объем 0,9%, а углекислый газ – 0,03%. Воздух также содержит примеси, такие как неон, криптон, метан, гелий, водород и ксенон.
В производственных помещениях большое значение предают аэроионному составу воздуха. Имеющиеся в воздухе отрицательно заряженные ионы благоприятно влияют на организм человека, заряжают его энергией, повышают настроение.
Азот
Азот – основной компонент воздуха. Перевод названия элемента – «неживой» – может относиться к азоту как к единому веществу, однако азот в связанном состоянии является одним из основных элементов жизни и входит в состав белков, нуклеиновых кислот, витаминов и т д.
Азот – элемент второго периода, не имеет возбужденных состояний, так как атом не имеет свободных орбиталей. Однако азот способен проявлять в основном состоянии не только III, но и IV валентность за счет образования ковалентной связи по донорно-акцепторному механизму с участием неподеленной электронной пары азота. Степень окисления, которую может проявлять азот, варьируется в широких пределах: от -3 до +5.
В природе азот встречается в виде одного вещества – газа N2 и в связанном состоянии. В молекуле азота атомы соединены прочной тройной связью (энергия связи 940 кДж/моль). При обычных температурах азот может реагировать только с литием. После предварительной активации молекул нагреванием, облучением или действием катализаторов азот реагирует с металлами и неметаллами.
Кислород
Кислород — самый распространенный элемент на Земле: массовая доля в земной коре — 47,3 %, объёмная доля в атмосфере — 20,95 %, массовая доля в живых организмах — около 65%.
Почти во всех соединениях (кроме соединений с фтором и пероксидами) кислород проявляет постоянную валентность II и степень окисления 2. Атом кислорода не имеет возбужденных состояний, так как на втором внешнем уровне отсутствуют свободные орбитали. Как единое вещество кислород существует в виде двух аллотропных модификаций — газов кислорода О2 и озона О3. Важнейшим соединением кислорода является вода. Около 71% поверхности Земли занято водой, без воды жизнь невозможна.
Озон в природе образуется из кислорода воздуха при грозовых разрядах, а в лаборатории — при пропускании электрического разряда через кислород.

Озон – еще более сильный окислитель, чем кислород. В частности? он окисляет золото и платину
Кислород в промышленности обычно получают сжижением воздуха с последующим отделением азота за счет его испарения (имеется разница в температурах кипения: -183 градуса для жидкого кислорода и -196 градусов для жидкого азота.)
Что мы узнали?
Воздух – необходимый элемент для каждого живого существа, значение которого сложно переоценить. Большую часть составляют азот и кислород. В химический состав воздуха также входят углекислый газ, аргон, неон, криптон, водород и гелий. В этой статье по химии (класс 8) кратко рассказывается о воздухе в целом и его основных элементах.








Комментирование закрыто