
Производные карбоновых кислот или неорганических кислот, в которых атом водорода в гидроксильной группе заменен радикалом, называются сложными эфирами. Обычно общую формулу сложных эфиров обозначают двумя углеводородными радикалами, присоединенными к карбоксильной группе — CnH2n+1-COO-CnH2n+1 или R-COOR’.
Номенклатура
Названия сложных эфиров состоят из названий радикала и кислоты с суффиксом «-ат». Например:
- CH3COOH – метилформиат;
- HCOOCH3 – этилформиат;
- CH3COOC4H9 – бутилацетат;
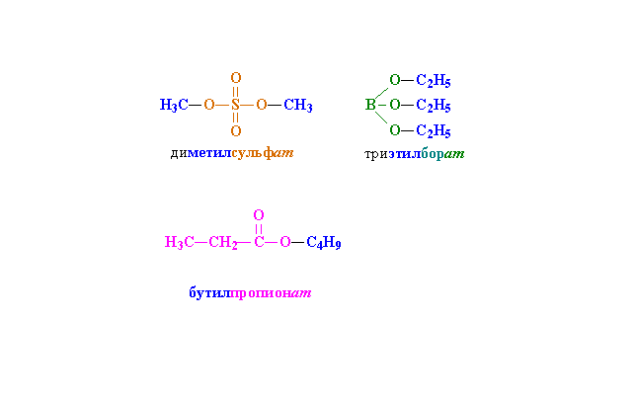
- CH3-CH2-COO-C4H9 – бутилпропионат;
- CH3-SO4-CH3 – диметилсульфат.
Также используются тривиальные названия кислот в соединении:
- С3Н7СООС5Н11 – амиловый эфир масляной кислоты;
- HCOOCH3 – метиловый эфир муравьиной кислоты;
- CH3-COO-CH2-CH(CH3)2 – изобутиловый эфир уксусной кислоты.
Классификация
В зависимости от происхождения сложные эфиры делятся на две группы:
- эфиры карбоновых кислот – содержат углеводородные радикалы;
- эфиры неорганических кислот – включает остальные минеральные соли (C2H5OSO2OH, (CH3O)P(O)(OH)2, C2H5ONO).
Наиболее разнообразны эфиры карбоновых кислот. Их физические свойства зависят от сложности их строения. Эфиры низших карбоновых кислот — летучие жидкости с приятным ароматом, а эфиры высших карбоновых кислот — твердые вещества. Это плохо растворимые соединения, плавающие на поверхности воды.
Виды эфиров карбоновых кислот приведены в таблице.
|
Вид |
Описание |
Примеры |
|
Фруктовые эфиры |
Жидкости, молекулы которых содержат не более восьми атомов углерода. Имеют фруктовый аромат. Состоит из одноатомных спиртов и карбоновых кислот |
|
|
Толстый |
Жидкости (масла) и твердые вещества, содержащие от девяти до 19 атомов углерода. Состоит из глицерина и карбоновой кислоты (остатки жирных кислот |
Оливковое масло представляет собой смесь глицерина с остатками пальмитиновой, стеариновой, олеиновой и линолевой кислот |
|
Растущий |
Твердые вещества с 15-45 атомами углерода |
CH3(CH2)14-CO-O-(CH2)29CH3 – мирицилпальмитат |

Сложные эфиры карбоновых кислот – главная составляющая ароматных эфирных масел, которые содержатся в плодах, цветах, ягодах. Также входят в состав пчелиного воска.

Получение
Эфиры готовят несколькими способами:
- реакция этерификации карбоновых кислот спиртами:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O;
- реакция ангидридов карбоновых кислот со спиртами:
(СН3СО)2О + 2С2Н5ОН → 2СН3СООС2Н5 + Н2О;
- реакция солей карбоновых кислот с галогенированными углеводородами:
CH3(CH2)10COONa + CH3Cl → CH3(CH2)10COOCH3 + NaCl;
- реакция присоединения карбоновых кислот к алкенам:
CH3COOH + CH2=CH2 → CH3COOCH2CH3 + H2O.
Свойства
Химические свойства сложных эфиров обусловлены функциональной группой -СООН. Основные свойства эфиров описаны в таблице.
|
Реакция |
Описание |
Уравнение |
|
Гидролиз |
При нагревании в воде они распадаются на кислоту и спирт. Под действием раствора щелочи образуются соль и спирт |
|
|
Галогенирование |
Реакция возможна при наличии кратных связей |
CH2=CH-C(O)-O-CH3 + Br2 → Br-CH2-C(Br)HC(O)-O-CH3 |
|
Замена |
Радикалы заменяются спиртовыми остатками и аминогруппами |
|
Сложные эфиры используются в косметологии, медицине, пищевой промышленности в качестве ароматизаторов, растворителей, наполнителей.
Что мы узнали?
Из темы урока химии в 10 классе мы узнали, что такое сложные эфиры. Это соединения, содержащие два радикала и карбоксильную группу. В зависимости от происхождения они могут содержать остатки минеральных или карбоновых кислот. Эфиры карбоновых кислот делятся на три группы: жировые, восковые, фруктовые эфиры. Это плохо растворимые в воде вещества с небольшой плотностью и приятным ароматом. Эфиры реагируют со щелочами, водой, галогенами, спиртами и аммиаком.








Комментирование закрыто