
Вещества, состоящие из углеродного скелета, полностью занятого атомами водорода, называются насыщенными или насыщенными углеводородами. К ним относятся два схожих класса веществ — линейные алканы и циклические циклоалканы. Общая химическая формула алканов – CnH2n+2, циклоалканов – CnH2n.
Строение
Алканы и циклоалканы находятся в состоянии sp3-гибридизации. Углерод связан с водородом одинарными σ-связями, образуя тетраэдр.
Молекулы алканов состоят из линейно присоединенных метиленовых групп -СН2, соединенных связями -СС. Метильная группа -СН3 может быть присоединена к любому атому углерода, образуя разветвленные цепи.
Молекулы циклоалканов образуются по тому же принципу, но цепи замыкаются в кольцо. Форма кольца или цикла зависит от количества атомов углерода: чем больше атомов, тем сложнее форма.
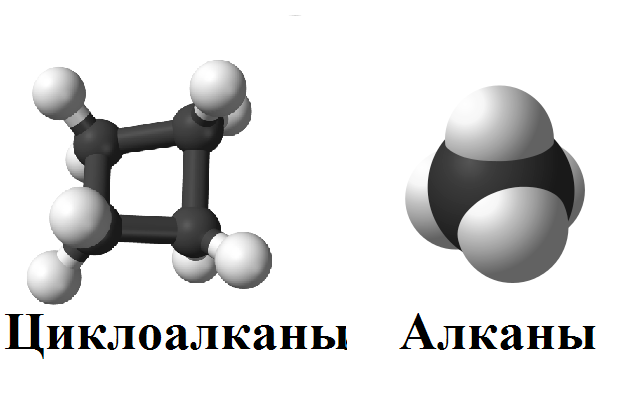
Дополнительные группы в структурной формуле записывают через черту или в скобочках. Циклоалканы обозначают геометрической фигурой, в углах которой по умолчанию находятся группы -CH2.
Гомологи и номенклатура
Названия веществ составлены по номенклатуре ИЮПАК следующим образом:
- алканы — греческий термин, обозначающий число (число атомов углерода) с суффиксом «-ан»;
- циклоалканы — названия алканов с приставкой «цикло-».
Простейший алкан — метан — содержит один атом углерода. Они образуют гомологический ряд алканов. Простейшим циклоалканом является циклопропан, имеющий форму треугольника.
Гомологические ряды предельных углеводородов и их физические свойства приведены в таблице.
|
Сорт |
Гомологи |
Формула вещества |
Физические свойства |
|
Алканы |
Метан |
CH4 |
Газы |
|
Этан |
C2H6 |
||
|
Пропан |
C3H8 |
||
|
Бутан |
C4H10 |
||
|
Пентан |
C5H12 |
Жидкости |
|
|
Гексан |
C6H14 |
||
|
Гептан |
C7H16 |
||
|
Октановое число |
C8H18 |
||
|
Нонан |
C9H20 |
||
|
Дин |
С10Н22 |
||
|
Ундиан |
C11H24 |
||
|
Додеканес |
C12H26 |
||
|
Тридекан |
C13H28 |
||
|
Тетрадекан |
C14H30 |
||
|
Пентадекан |
C15H32 |
||
|
Гексадекан |
C16H34 |
Твердые вещества |
|
|
Циклоалканы |
Циклопопропан |
C3H6 |
Газы |
|
Циклобутан |
C4H8 |
||
|
Циклопентан |
C5H10 |
Жидкости |
|
|
Циклогексан |
C6H12 |
||
|
Циклогептан |
C7H14 |
||
|
Циклооктан |
C8H16 |
||
|
Циклононан |
C9H18 |
||
|
Циклодекан |
С10Н20 |
||
|
Циклон декан |
C11H22 |
||
|
Циклододекан |
C12H24 |
Твердые вещества |
Плотность алканов не превышает единицы, поэтому соединения плавают на поверхности воды. Температуры плавления и кипения увеличиваются с увеличением молекулярной массы. Плотность, температуры плавления, кипения циклоалканов выше, чем у алканов.
Изомерия
Алканам, начиная с бутана, свойственна изомерия углеродного скелета, а начиная с гептана — оптическая изомерия.
При изомерии углеродного скелета или структурной изомерии к атомам углерода в основной цепи добавляются дополнительные группы. Это меняет название веществ. Сначала указываются номера атомов, к которым присоединены группы, затем названия групп и полное название основной цепи. Тривиальные имена образуются с помощью префикса «изо-». Бутан образует, например, изобутан или 2-метилпропан — СН3-СН(СН3)-СН3.
Оптическая изомерия — это образование стереоизомеров, зеркально отражающих друг друга.
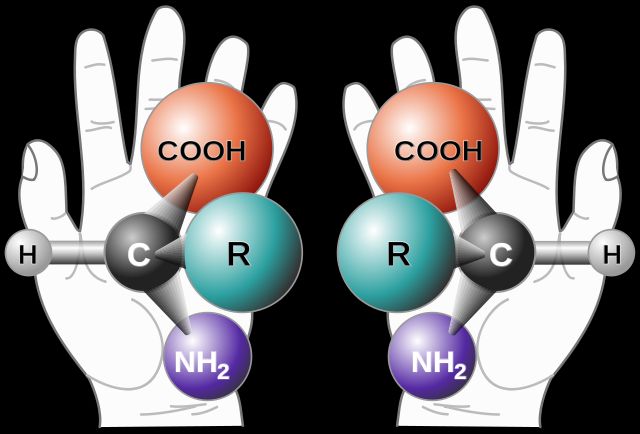
Циклоалканы характеризуются тремя типами изомерии:
- углеродный скелет – присоединение -CH2 или боковых цепей;
- пространственный – расположение относительно плоскости цикла;
- межклассовые – образование изомеров с алкенами.

Количество изомеров возрастает с увеличением числа атомов углерода в гомологическом ряду. Например, октан (C8H18) имеет 18 изомеров, а гектан (C100H202) – 5,921·1039. Теоретическое число изомеров высчитывается по специальной формуле.
Свойства
Насыщенные углеводороды активны под действием температуры и катализаторов. Они подвергаются реакциям присоединения и замещения. Химические свойства циклоалканов зависят от количества атомов углерода в молекуле вещества. Ниже приведены основные свойства предельных углеводородов.
|
Реакция |
Алканы |
Циклоалканы |
|
Галогенирование |
CH4 + Cl2 → CH3Cl + HCl |
|
|
Гидрирование |
– |
C4H8 + H2 -> СН3-СН2-СН2-СН3 |
|
Добавление галогеноводородов |
– |
C3H6 + HI → CH3-CH2-CH2I |
|
Дегидрирование |
СН3-СН3 -> СН2=СН2 + H2 |
C6H12 ↔ C6H6 + 3H2 |
|
Окисление |
CH4 + 2O2 → CO2 + 2H2O |
C6H12 + 2O2 ↔ C6H10O4 |
|
Азотирование |
CH4 + HNO3 → CH3NO2 + H2O |
– |
|
Разложение |
C6H14 -> C6H6 + 4H2 |
– |
Что мы узнали?
На уроке химии в 10 классе мы узнали, что такое предельные или предельные углеводороды. К ним относятся алканы и циклоалканы со схожими физическими и химическими свойствами. Алканы – это ациклические линейные углеводороды, образующиеся из метана. Простейшим представителем циклических алканов является циклопропан. Для веществ характерна изомерия по углеродному скелету, а также оптическая изомерия для алканов, основанная на гептане, межклассовая и пространственная изомерия для циклоалканов. Простейшие предельные углеводороды — газы, высшие — твердые вещества. Соединения подвергаются реакциям присоединения, замещения и окисления.








Комментирование закрыто