
Кислород появился в атмосфере Земли с появлением зеленых растений и фотосинтезирующих бактерий. Благодаря кислороду аэробные организмы осуществляют дыхание или окисление. Важно получать кислород в промышленности – его используют в металлургии, медицине, авиации, народном хозяйстве и других отраслях.
Свойства
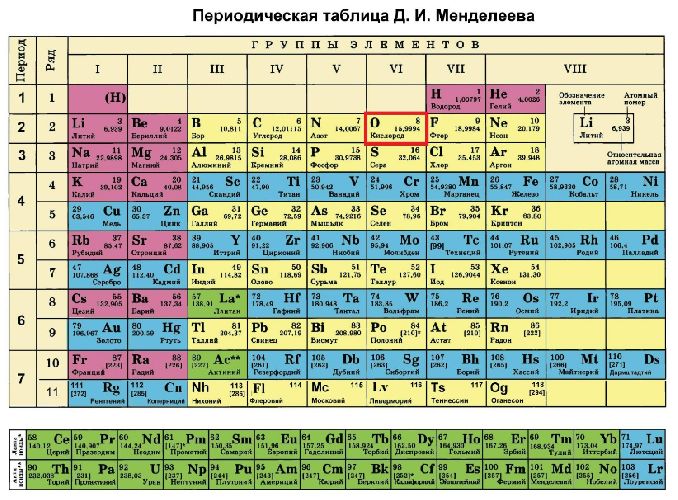
Кислород — восьмой элемент таблицы Менделеева. Это газ, поддерживающий горение и окисляющий вещества.
Официально кислород был открыт в 1774 году. Английский химик Джозеф Пристли выделил этот элемент из оксида ртути:
Однако Пристли не знал, что кислород входит в состав воздуха. Свойства и наличие кислорода в атмосфере позже определил коллега Пристли, французский химик Антуан Лавуазье.
Общие свойства кислорода:
- бесцветный газ;
- не имеет запаха и вкуса;
- тяжелее воздуха;
- молекула состоит из двух атомов кислорода (О2);
- в жидком состоянии имеет бледно-голубой цвет;
- плохо растворяется в воде;
- является сильным окислителем.

Присутствие кислорода легко проверить, опустив в сосуд с газом тлеющую лучину. При наличии кислорода лучина вспыхивает.
Как получают
Известно несколько способов получения кислорода из различных соединений в промышленных и лабораторных условиях. В промышленности кислород получают из воздуха путем его сжижения под давлением и при температуре -183°С. Жидкий воздух подвергается испарению, т е постепенно нагревается. При -196°С азот начинает испаряться, а кислород остается жидким.
В лаборатории кислород образуется из солей, перекиси водорода и в результате электролиза. Расщепление солей происходит при нагревании. Например, хлорат калия или бертолитовую соль нагревают до 500 °С, а перманганат калия или перманганат калия — до 240 °С:
- 2KClO3 → 2KCl + 3O2↑;
- 2KMnO4 → K2MnO4 + MnO2 + O2↑.

Получить кислород также можно путем нагревания нитрата или нитрата калия:
При расщеплении пероксида водорода в качестве катализатора используют оксид марганца (IV) – MnO2, углерод или порошок железа. Общее уравнение выглядит следующим образом:
Раствор гидроксида натрия подвергается электролизу. В результате образуются вода и кислород:
Кислород также выделяют из воды с помощью электролиза, расщепляя его на водород и кислород:
На атомных подводных лодках кислород получали из пироксида натрия – 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑. Способ интересен тем, что вместе с выделением кислорода поглощается углекислый газ.
Как применяют
Сбор и распознавание необходимы для выделения чистого кислорода, который используется в промышленности для окисления веществ, а также для поддержания дыхания в космосе, под водой и в задымленных помещениях (кислород необходим пожарным). В медицине кислородные баллоны помогают пациентам с затрудненным дыханием дышать. Кислород также используется для лечения респираторных заболеваний.
Кислород используется для сжигания топлива – угля, нефти, природного газа. Кислород широко используется в металлургии и машиностроении, например, для плавки, резки и сварки металла.
Что мы узнали?
Кислород — бесцветный газ, необходимый для дыхания и используемый в промышленности. Кислород получают сжижением и испарением воздуха, электролизом воды или гидроксида натрия, выделяют из солей и перекиси водорода. Кислород используется для поддержания дыхания в местах с ограниченным или полным отсутствием кислорода, а также в отраслях сжигания топлива и производства металлов.








Комментирование закрыто