
Оксиды – неорганические вещества, одним из элементов которых обязательно является кислород в степени окисления -2. Оксиды могут быть солеобразующими и несолеобразующими: одним из типов солеобразующих оксидов являются кислотные оксиды. Каковы их свойства и о каких характерных свойствах кислотных оксидов следует знать?
Характеристика кислотных оксидов
Кислотные оксиды – это оксиды неметаллов или переходных металлов в высоких степенях окисления (от +4 до +7). Кислотные оксиды (ангидриды) проявляют кислотные свойства и образуют кислородсодержащие кислоты. Следовательно, кислотным оксидам соответствуют кислоты. Например, кислотным оксидам SO2, SO3 соответствуют кислоты H2SO3 и H2SO4 .

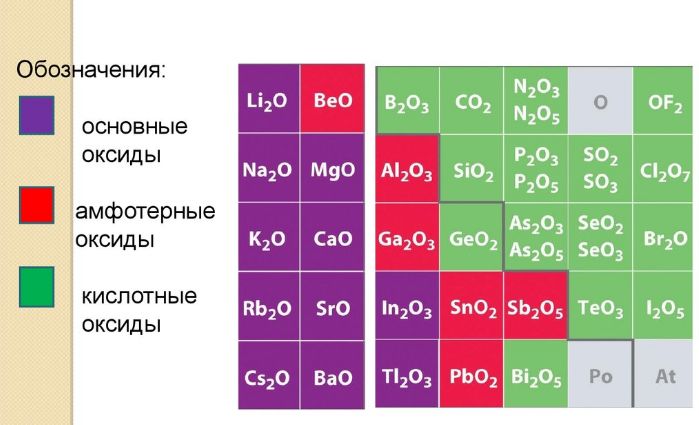
Если кислотный оксид имеет высшую степень окисления, то его относят к высшим оксидам. В периоде слева направо металлические свойства химических элементов ослабевают, соответственно, кислотные свойства высших оксидов и их гидратов постепенно изменяются от основных к кислотным (кислотные свойства оксидов и их гидратов слева направо в периоде усиливаются).
Химические свойства кислотных оксидов
Кислотные оксиды обладают рядом химических свойств:
- Кислотные оксиды реагируют с водой, в результате чего образуются кислоты:
Cуществуют оксиды, которые не вступают в реакцию с водой, например, оксид кремния – SiO2
- Кислотные оксиды могут взаимодействовать с другими видами оксидов – основными, образуя соли:
- Кислотные оксиды взаимодействуют также с основаниями, в результате чего образуются соли:
- Если этому оксиду соответствует многоосновная кислота, то может образоваться и кислая соль:
- Нелетучие кислые оксиды в солях обладают способностью замещать летучие оксиды:
- Кислотные оксиды могут образовываться при разложении в результате нагревания сложных веществ, содержащих кислород – кислот, нерастворимых оснований, солей:

Что мы узнали?
Кислотные оксиды – это вещества, образованные из атомов кислорода и неметаллов или переходных металлов. Они могут взаимодействовать и реагировать с водой, основные оксиды, основания и нелетучие оксиды обладают способностью замещать летучие оксиды в солях.








Комментирование закрыто