
Физические свойства металлов отличают их от неметаллов. Все металлы, кроме ртути, представляют собой твердые кристаллические вещества, являющиеся восстановителями в окислительно-восстановительных реакциях.
Положение в таблице Менделеева
Металлы занимают I-II группы и боковые подгруппы III-VIII групп. Металлические свойства и т.д.способность отдавать валентные электроны или окислять увеличивается сверху вниз по мере увеличения количества энергетических уровней. Слева направо металлические свойства ослабевают, поэтому наиболее активные металлы находятся в I-II группах, основных подгруппах. Это щелочные и щелочноземельные металлы.
Определить степень активности металлов можно по электрохимическому ряду напряжений. Металлы, стоящие до водорода, наиболее активны. После водорода стоят слабоактивные металлы, не вступающие в реакцию с большинством веществ.

Строение
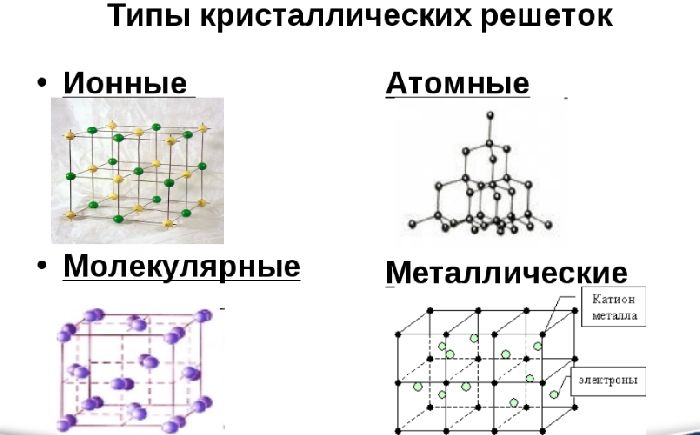
Независимо от активности все металлы имеют общее строение. Атомы в простом металле расположены не хаотично, как в аморфных веществах, а упорядоченно – в виде кристаллической решетки. Металлическая связь удерживает атомы в одном положении.
Такой тип связи осуществляется за счет положительно заряженных ионов, расположенных в узлах кристаллической ячейки (узла решетки), и отрицательно заряженных свободных электронов, образующих так называемый электронный газ. Электроны отделились от атомов, превратив их в ионы, и начали хаотично двигаться в решетке, связывая ионы между собой. Без электронов решетка разрушилась бы из-за отторжения одинаково заряженных ионов.
Различают три типа кристаллической решётки. Кубическая объемно-центрированная состоит из 9 ионов и характерна хрому, железу, вольфраму. Кубическая гранецентрированная включает 14 ионов и свойственная свинцу, алюминию, серебру. Из 17 ионов состоит гексагональная плотноупакованная решётка цинка, титана, магния.
Свойства
Строение кристаллической решетки определяет основные физические и химические свойства металлов. Металлы блестят, плавятся, проводят тепло и электричество. Промышленность и металлургия нашли перемены в физических производных металлов в изделиях, фольге, корпусах машин, зеркалах, бытовой и промышленной химии. Свойства металлов и их применение представлены в таблице физических свойств металлов.
|
Характеристики |
Функции |
Примеры |
Приложение |
|
Металлический блеск |
Способность отражать солнечный свет |
Наиболее блестящие металлы — Hg, Ag, Pd |
Изготовление зеркал |
|
Плотность |
Легкие – имеют плотность менее 5 г/см3 |
На, К, Ба, Мг, Ал. Самый легкий металл — литий плотностью 0,533 г/см3 |
Изготовление облицовки, детали работ |
|
Тяжёлые – имеют плотность более 5 г/см3 |
Sn, Fe, Zn, Au, Pb, Hg. Самый тяжёлый – осмий с подсветкой 22,5 г/см3 |
Использование на плотах |
|
|
Пластичность |
Возможность изменения формы без повреждений |
Самые пластичные – Au, Cu, Ag. Хрупкие – Zn, Sn, Bi, Mn |
Формовка, гибка труб, изображение проволоки |
|
Твердость |
Мягкие – режутся ножом |
Ну, К, В |
Производство мыла, стекла, удобрений |
|
Твёрдые – сновимы по твёрдости с алмазом |
Самый твёрдый – хром, режет стекло |
Изготовление несуществующих конструкций |
|
|
Температура плавления |
Легкоплавкие – температура плавления ниже 1000°С |
Hg (38,9°С), Ga (29,78°С), Cs (28,5°С), Zn (419,5°С) |
Производитель радиотехники, жести |
|
Тугоплавкие – температура плавления выше 1000°С |
Cr (1890°С), Mo (2620°С), V (1900°С). Самый тугоплавкий – вольфрам (3420°С) |
Производство ламп накаливания |
|
|
Теплопроводность |
Способность передавать тепло другим телам |
Лучшими проводниками тока и тепла являются Ag, Cu, Au, Al |
Приготовление еды в металлической посуде |
|
Електропроводность |
Способность проводить электрический ток за счет свободных электронов |
Передача электричества по проводам |
Что мы узнали?
На уроке 9 класса они узнали о физических свойствах металлов. Они кратко рассмотрели положение металлов в таблице Менделеева и особенности строения кристаллической решетки. Благодаря своей структуре металлы обладают пластичностью, твердостью, способностью плавиться, проводить электрический ток и тепло. Свойства металлов неоднородны. Различают легкие и тяжелые металлы, легкоплавкие и твердоплавкие, мягкие и твердые. Физические свойства используются для производства плотов, электрических проводов, посуды, мыла, стекла, конструкций различной формы.








Комментирование закрыто