
Фенол – простейший представитель ароматического ряда фенолов. От бензола он отличается наличием гидроксильной группы -ОН. Другие названия: гидроксибензол, карболовая кислота. Формула – C6H5OH.
Строение
Благодаря наличию бензольного кольца фенол относят к ароматическим углеводородам (аренам). Однако один атом водорода заменен на гидроксильную группу, поэтому фенол не относится к бензольному ряду. Структурная формула фенола изображается как молекула бензола с присоединенной группой -ОН.
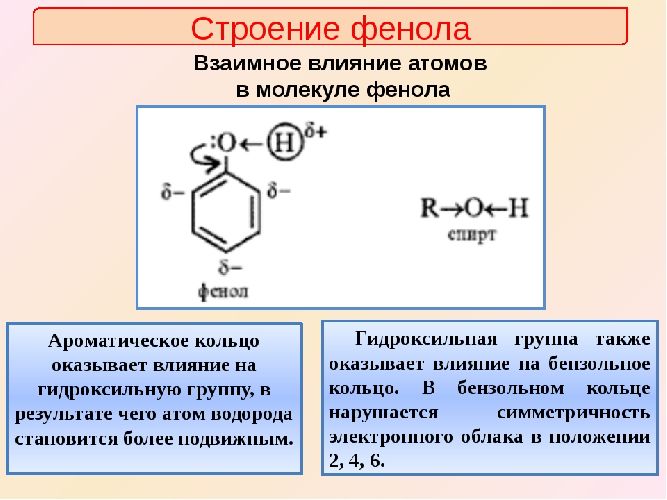
Классификация
Фенолы различаются по количеству гидроксильных групп. В бензольном кольце один, два, три и более атомов водорода могут быть заменены группой -ОН. Поэтому выделяются фенолы:
- одноатомные – аренолы (фенол и его гомологи);
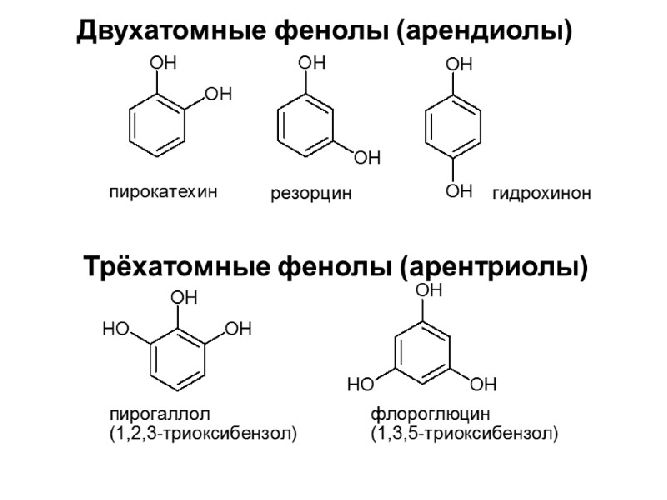
- двухатомные – арендиолы (пирокатехин, резорцин, гидрохинон);
- трехатомные – арендтриолы (флороглюцинол, пирогаллол);
- многоатомный.
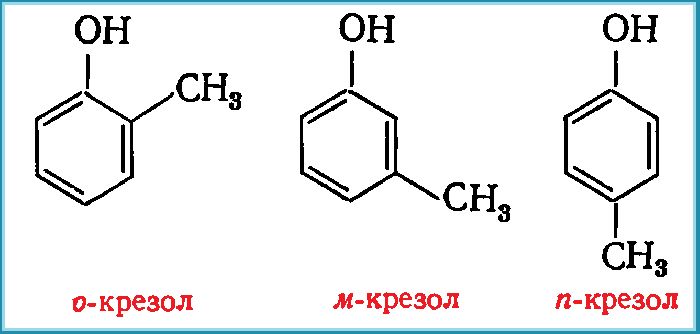
Фенол образует гомологический ряд с общей формулой CnH2n-7OH, где n равно не менее шести. Наиболее известными гомологами являются крезол (C7H7OH) и этилфенол (C8H9OH).
Кроме того, фенолы классифицируются по числу ароматических колец (бензольных колец). Фенол и его гомологи имеют только одно бензольное кольцо. Также отлично:
- нафтолы – содержат два ароматических ядра;
- антролы – состоит из трех бензольных колец;
- фенантролы – включает четыре ароматических ядра;
- бензотетролы – содержат пять бензольных колец.
Названия фенолов включают:
- числовой список атомов углерода, к которым присоединены заместители и гидроксильные группы;
- префикс, указывающий количество заместителей и групп -ОН;
- приставка «гидрокси-»;
- имя зам.
Каждое структурное название заканчивается словом «бензол». Например, 1-гидрокси-2-метилбензол. Это означает, что к первому атому углерода присоединена гидроксильная группа, а ко второму — метильная группа.
Другие примеры:
- 1,2,3-тригидроксибензол;
- 1,3 – дигидроксибензол;
- 1-гидрокси-4-метилбензол.
Большинство фенолов имеют тривиальные названия.
Для фенолов характерна структурная изомерия по положению заместителей в бензольном кольце, по строению и количеству радикалов.
Физические свойства
Фенол в обычных условиях представляет собой игольчатые бесцветные кристаллы, розовеющие на воздухе. Это токсичное вещество, вызывающее ожоги.
Основные физические свойства вещества:
- растворимость в воде – 6 г на 100 мл;
- температура плавления – 43°С;
- температура кипения – 183°С;
- плотность – 1,07 г/см3 (тяжелее воды);
- молекулярная масса – 94,11 г/моль.
Фенол получают путём окисления кумола или толуола. Также выделяют из каменноугольной смолы.
Химические свойства
По реакционной способности фенола можно разделить на три группы:
- за счет ОН-связи (кислотные свойства);
- по бензольному кольцу (реакции замещения);
- качественные реакции.
Важнейшие химические свойства фенола представлены в таблице.
|
Реакция |
Описание |
Уравнение |
|
С активными металлами и щелочами |
Образование солей – фенолятов |
|
|
Азотирование |
Под действием разбавленной азотной кислоты образуется смесь нитрофенолов (орто- и пара-). При воздействии концентрированной кислоты образуется пикриновая кислота (2,4,6-тринитрофенол) |
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 2H2O |
|
Галогенирование |
При комнатной температуре 2,4,6-трибромфенол образуется в виде белого осадка |
C6H5OH + 3Br2 → C6H3Br3O + 3HBr |
|
Гидрирование |
Под воздействием температуры в присутствии катализатора (никеля) образуется циклогексанол |
C6H5OH + 3H2 → C6H11OH |
|
Высокое качество |
Обнаружение с использованием хлорида железа(III). Образуется раствор фиолетового цвета |
6 C6H5OH + FeCl3 → [Fe(C6H5OH)3](C6H5O)3 + 3HCl |
Что мы узнали?
Из урока химии мы узнали, что фенол – ароматическое соединение, образующее разнообразные фенолы. Он отличается от бензола наличием гидроксильной группы. В зависимости от числа групп различают одноатомные, двухатомные, трехатомные и многоатомные фенолы. Соединения также могут содержать более одного бензольного кольца. Фенол – токсичное кристаллическое вещество с низкой температурой плавления и кипения. Реакции происходят по гидроксильной группе и бензольному кольцу. Фенол реагирует с активными металлами, щелочами, азотной кислотой, галогенами и водородом. Наличие фенола определяется качественной реакцией — действием хлорида железа(III).








Комментирование закрыто