
Металлическая связь образуется между атомами в кристалле металла в результате перекрывания валентных электронов. Итак, что же это за соединение и в каких соединениях оно присутствует?
Что такое металлическая связь?
Металлическая химическая связь существует в кристалле металла и в жидком расплавленном состоянии. Его образуют элементы, атомы которых на внешнем уровне имеют мало электронов (1-3) по сравнению с общим числом внешних, энергетически близких орбиталей.

Валентные электроны из-за малой энергии ионизации слабо удерживаются в атоме. Таким образом, атом натрия имеет 9 свободных и энергетически близких орбиталей на один валентный электрон (3S1) (одну 3s, три 3p и пять 3d). Из-за малого значения энергии ионизации валентный электрон удерживается слабо и свободно перемещается не только в пределах своих 9 свободных орбиталей, но и плотно упакованных в кристалле и в свободных орбиталях других атомов, образуя соединение.
Химическая связь сильно делокализована: электроны разделяются («электронный газ») и движутся через кусок металла, который обычно электрически нейтрален, между положительно заряженными ионами.
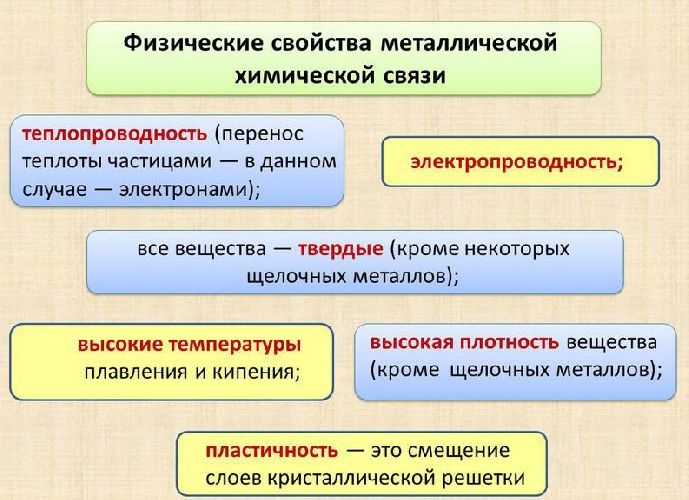
Свободное перемещение электронов по кристаллу объясняет ненаправленность и ненасыщенность связи, а также такие физические свойства металлов, как пластичность, блеск, электро- и теплопроводность.
Характерные кристаллические решетки
Металлы почти всегда образуют высокосимметричные решетки, в которых атомы плотно упакованы вместе. Различают три типа кристаллических решеток:
- объемноцентрированная кубическая. В решетке этого типа атомы располагаются на вершине куба, а один атом находится в центре объема куба. Такую решетку имеют следующие металлы: натрий, литий, барий, калий, свинец и многие другие.
- гранецентрированный куб. В решетке этого типа атомы располагаются в верхней части куба и в центре каждой стороны. Такой тип решетки имеют следующие металлы: церий, стронций, никель, серебро, золото, палладий, платина, медь и многие другие.
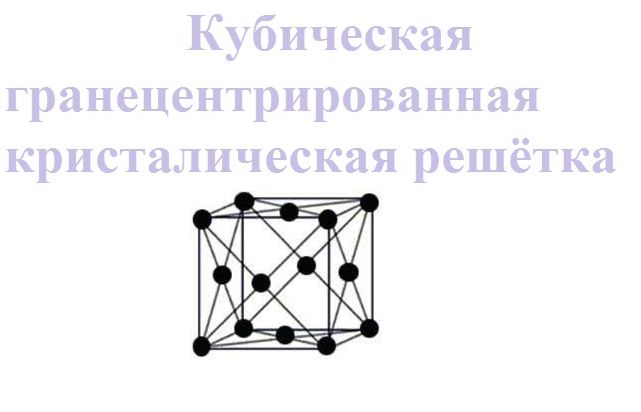
- шестиугольный. В решетке этого типа атомы расположены вверху и в центрах шестиугольного основания призмы, а три атома расположены в средней плоскости этой призмы.
Такой тип кристаллической решетки имеют следующие металлы: магний, кадмий, рений, осмий, рутений, бериллий и многие другие.
Что мы узнали?
Металлическая связь по своей природе близка к ковалентной связи, но отличается от нее тем, что обмен электронами при ее образовании осуществляется многими атомами одновременно. В данной статье дано определение понятия «металлическая связь», а также приведены примеры металлических химических связей.








Комментирование закрыто