
Металлы – особая группа элементов периодической таблицы Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твердостью и эластичностью, что обусловлено кристаллической структурой металлов.
Общее строение
Металлы – это твердые тела с кристаллической структурой. Исключением является ртуть, жидкий металл. Кристаллические решетки представляют собой атомы металлов, расположенные определенным образом. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. Атомам металлов не хватает электронов, поэтому они являются ионами.
Единицей кристаллической решетки является элементарная кристаллическая ячейка, в условных узлах и на поверхности которой находятся положительно заряженные ионы. Они удерживаются вместе металлическими связями, возникающими вследствие хаотического движения электронов, отделившихся от атомов (благодаря чему атомы превратились в ионы). Отрицательно заряженные электроны удерживают положительно заряженные электроны на равном расстоянии, придавая кристаллической решетке правильную геометрическую форму.
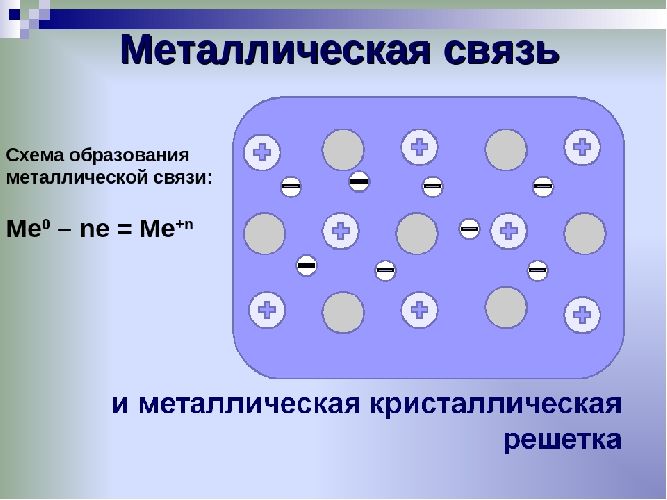
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Виды решёток
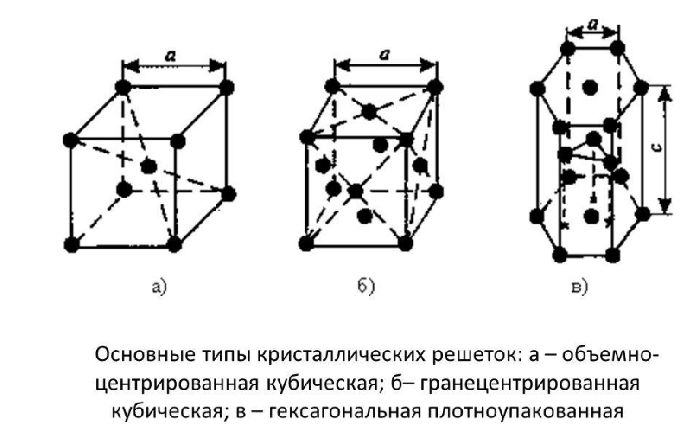
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решеток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
BCC — это куб с атомами в узлах. Девятый ион расположен в центре куба, на пересечении диагоналей. Этот тип характерен для железа, молибдена, хрома, вольфрама и ванадия.
Элементарная кристаллическая ячейка ГЦК-типа представляет собой куб с ионами в узлах и в центре каждой грани — на пересечении диагоналей. Такую структуру имеют медь, серебро, алюминий, свинец и никель.
Третий тип имеет форму шестиугольной призмы, в узлах которой находится по шесть ионов с каждой стороны. Один ион расположен посередине между шестью узлами. В центре призмы между шестиугольными гранями находится равносторонний треугольник, состоящий из трех ионов.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Характеристика решётки
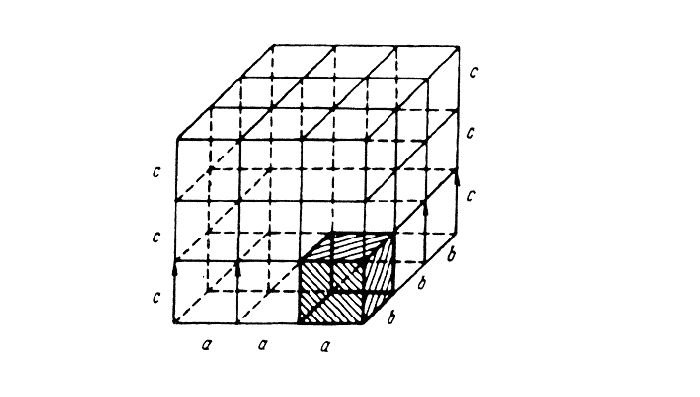
Кристаллические решетки характеризуются компактностью или степенью наполненности. Компактность определяется следующими показателями:
- параметр решетки – расстояние между атомами;
- количество атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки — это отношение объема, занимаемого атомами, к общему объему решетки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
Что мы узнали?
Мы кратко узнали об атомно-кристаллическом строении металлов. Металлы – твердые кристаллические вещества. Единица решетки представляет собой кристаллическую элементарную ячейку. Благодаря металлическим связям ионы в межклеточных соединениях удерживаются на одинаковом расстоянии. Существует три типа кристаллической решетки — ОЦК, ГЦК и ГПУ, различающиеся числом атомов и геометрической формой.








Комментирование закрыто