
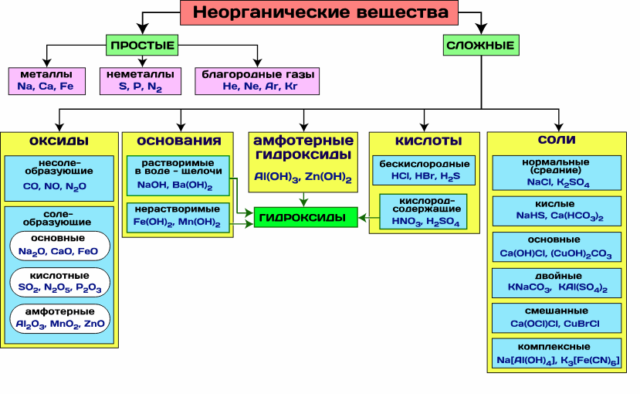
Классификация неорганических веществ основана на их способности к разложению. Простые вещества, состоящие из атомов только одного химического элемента (О2, Н2, Mg), не разлагаются. Сложные вещества, состоящие из атомов двух и более элементов (CO2, H2SO4, NaOH, KCl), легко распадаются).
Простые
Классификация классов неорганических веществ включает:
- металлы – элементы, обладающие тепло- и электропроводностью, высокой пластичностью, ковкостью и металлическим блеском;
- неметаллы – это элементы, которые более хрупкие, чем металлы, не проводят электричество и обладают окислительными свойствами.
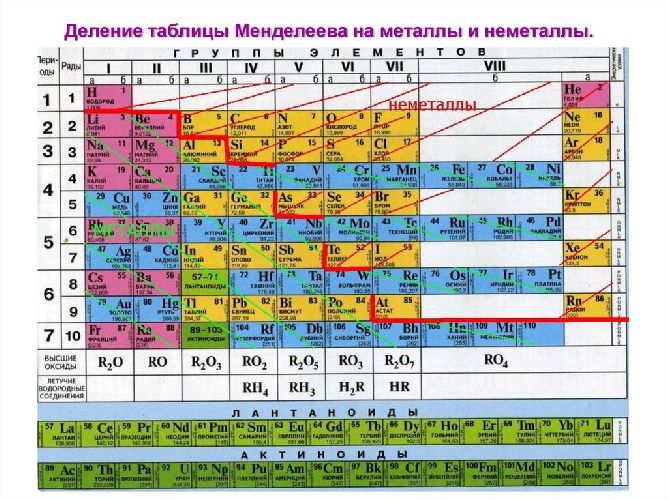
Металлы располагаются в левом нижнем углу таблицы Менделеева, неметаллы – в правом верхнем углу и включают в себя благородные газы.
Многие простые химические элементы обладают аллотропией – свойством образовывать несколько простых веществ. Например, при присоединении ещё одного атома к кислороду образуется простое вещество озон (О3), углерод в зависимости от количества атомов образует графит, уголь или алмаз.
Сложные
Сложные вещества классифицируют на следующие классы:
- оксиды – состоят из двух элементов, один из которых – кислород;
- кислоты – состоят из атомов водорода и кислотного остатка;
- основания – состоят из металла и одной или нескольких гидроксильных групп;
- соли – состоят из металла и кислотного остатка.
Отдельно выделяют амфотерные гидроксиды, проявляющие свойства кислот и оснований. Это твердые вещества, являющиеся слабыми электролитами. К ним относятся гидроксиды металлов со степенью окисления +3 и +4. Исключение составляют Be(OH)2, Zn(OH)2, Sn(OH)2, Pb(OH)2.
Более подробная классификация сложных веществ представлена в таблице примеров.
|
Вид |
Номенклатура |
Химические свойства |
Пример |
|
Оксиды — ЭксОй |
Оксид элемента (степень окисления) |
Существуют основные оксиды, образующие соли при взаимодействии с кислотами, и кислотные оксиды, образующие кислоты при взаимодействии с основаниями. Отдельно выделяют амфотерные оксиды, взаимодействующие с кислотами и основаниями (образуется соль) |
Na2O – оксид натрия, Fe2O3 – оксид железа (III), N2O5 – оксид азота (V) |
|
Основания – Me(OH)x |
Гидроксид металла (степень окисления) |
По растворимости различают щелочи и водонерастворимые основания. Щелочи реагируют с неметаллами и кислотными оксидами. Нерастворимые основания реагируют с кислотами и могут разлагаться при высоких температурах |
Fe(OH)2 – гидроксид железа(II), Cu(OH)2 – гидроксид меди(II), NaOH – гидроксид натрия |
|
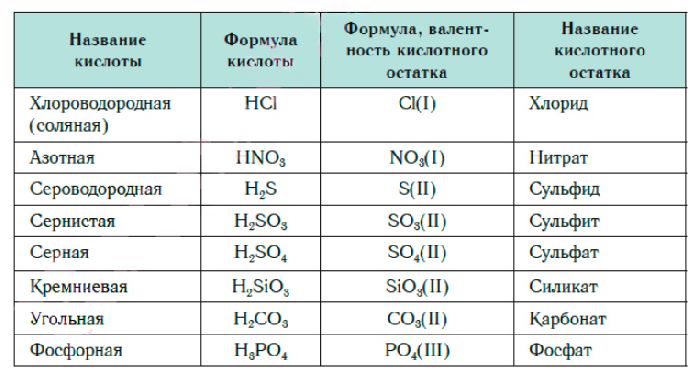
Кислоты – HnAc |
Читать в зависимости от кислотных остатков |
Они взаимодействуют с металлами слева от водорода в ряду активности, с оксидами и солями. Может разлагаться при высоких температурах |
H2SO4 – серная кислота, HCl – соляная кислота, HNO3 – азотная кислота |
|
Салтер – Пелс(Ак)у |
Кислотные остатки металла (степень окисления) |
Реагирует с кислотами, щелочами, металлами и солями |
Na2SO4 – сульфат натрия, CaCO3 – карбонат кальция, KCl – хлорид калия |
Генетические связи между классами основаны на взаимном превращении веществ. При химических реакциях атомы переходят от одного вещества к другому, образуя генетические ряды (ряды превращений). Металл при присоединении кислорода образует оксид, который при взаимодействии с водой превращается в основание. Из неметалла образуется кислотный оксид, который, взаимодействуя с водой, образует кислоту. Любой генетический ряд заканчивается солью.
Что мы узнали?
К неорганическим веществам относятся простые и сложные соединения. Простые вещества состоят из атомов одного и того же элемента. К ним относятся металлы и неметаллы. К комплексным соединениям относятся вещества, состоящие из нескольких элементов. К ним относятся оксиды, кислоты, основания, соли и амфотерные гидроксиды. Все вещества генетически связаны друг с другом. Из простого вещества можно получить более сложное вещество. Соли считаются сложнейшими веществами.








Комментирование закрыто