
Частица, содержащая разное количество протонов и электронов, называется ионом. Если число протонов больше, ион приобретает положительный заряд и становится катионом. Ионы с отрицательным зарядом (преобладают электроны) называются анионами.
Общее описание
Понятие «ион» впервые появилось в химии в 1834 году благодаря экспериментам Майкла Фарадея. Исследователь изучал электропроводность водных растворов кислот, солей и щелочей. Он предположил, что способность проводить электричество обусловлена движением заряженных частиц — ионов — в растворе.
Молекулы способны распадаться на ионы – атомы с недостатком или избытком электронов. Процесс разложения называется электролитической диссоциацией, а образующийся раствор или расплав — электролитом. Если погрузить электрод в раствор электролита, катионы начнут двигаться к катоду – отрицательному полюсу, а анионы – к аноду – положительному полюсу. Это объясняет электропроводность электролитов.
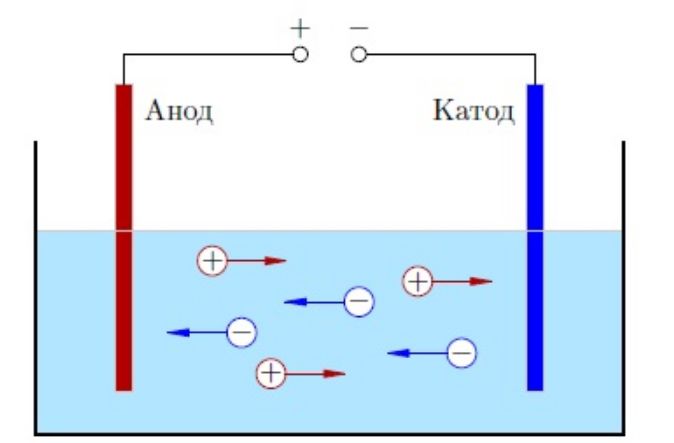
В растворах или в расплавах ионы образуются под действием молекул воды или высокой температуры.
Строение
Ионы состоят из ядра и электронов, которые движутся вокруг. Ядро состоит из положительно заряженных частиц (протонов) и нейтральных частиц (нейтронов). Число протонов совпадает с атомным номером элемента. Число нейтронов равно разнице между относительной атомной массой и числом протонов.
Электроны располагаются по энергетическим уровням. Число уровней совпадает с периодом, в котором находится элемент. Внешний энергетический уровень содержит валентные электроны, которые могут взаимодействовать с другими атомами. Когда атом теряет валентные электроны, он становится катионом; когда добавляется дополнительный электрон, он становится анионом.
Если, например, к атому хлора добавить еще один электрон, он станет отрицательно заряженным ионом — анионом. А если у атома натрия отобрать один электрон, он станет положительно заряженным ионом – катионом, потому что число протонов будет больше, чем отрицательных электронов.
Катионы в уравнениях отмечаются плюсом, а анионы – минусом. Например, Fe2+, Al3+, Na+, F–, Cl–. Цифра означает, сколько электронов отдал или принял атом, став ионом, т.е показывает степень окисления. Количество катионов или анионов можно посмотреть по таблице растворимости веществ.
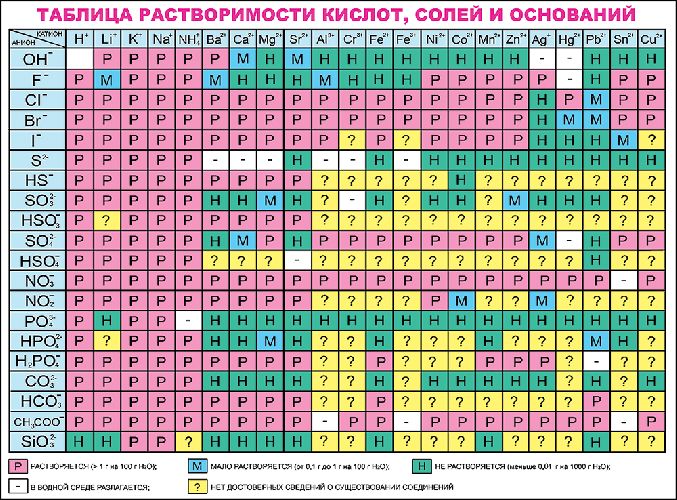
Классификация
Ионы делятся на две группы:
- простые или одноатомные – содержат одно ядро, т.е состоят из одного атома вещества;
- сложный или многоатомный – содержит не менее двух ядер, т.е состоит из двух и более атомов вещества.
К простым ионам относятся катионы и анионы металлов и неметаллов – Na+, Mg2+, Cl–. Сложные ионы образуются при соединении иона с нейтральными молекулами вещества. Например:
- NH3 + H+ → NH4+;
- БФ3 + Ф– → БФ4–.
Катионы – это ионы металлов, водорода, аммония и некоторых других веществ. Анионы – это гидроксид-ионы (ОН–), ионы кислотных остатков, неметаллов и других веществ.
Некоторые атомы могут стать катионами или анионами в зависимости от реакции.
Высвобождаются также ион-радикалы – свободные заряженные частицы, способные присоединяться к атомам или прикрепляться к атомам других веществ. В зависимости от заряда их разделяют на катион-радикалы и анион-радикалы.
Ионная связь – класс соединения ионов. Ионная связь возникает в результате электростатического притяжения анионов и катионов. При этом атом с большей электроотрицательностью притягивает атом с меньшей электроотрицательностью. Ионная связь возникает преимущественно между ионами металлов и неметаллов. Металл всегда отдаёт электроны, т.е является восстановителем.
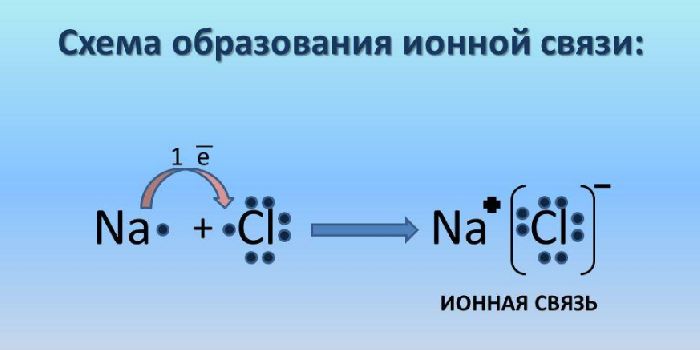
Что мы узнали?
Из темы урока мы узнали, что такое ионы. Атом становится ионом, когда электроны удаляются или добавляются. Если электронов меньше, атом приобретает положительный заряд за счет преобладания протонов и становится катионом. Когда число отрицательно заряженных электронов увеличивается, атом становится анионом. Ионы способны передавать электричество и обязательно присутствуют в электролитах. Ионная связь возникает между ионами вследствие электростатического притяжения отрицательно и положительно заряженных частиц.








Комментирование закрыто