Гидроксид кальция – химическое вещество, имеющее сильное основание. О каких его функциях и химических свойствах пойдет речь в этой статье.
Характеристика гидроксида кальция
Кристаллический гидроксид кальция представляет собой белый порошок, разлагающийся при нагревании, но практически нерастворимый в воде. Формула гидроксида кальция Ca(OH)2. В ионной форме уравнение образования гидроксида кальция выглядит так:
Гидроксид кальция имеет и другие названия: гашеная известь, известковое молоко, известковая вода
Молярная масса гидроксида кальция составляет 74,09 г/моль. Это значит, что в 74,09 г/моль гидроксида кальция содержится 6,02*10^23 атома или молекулы этого вещества.
Гидроксид кальция применяют для известкования в строительстве, дезинфекции стволов деревьев, в сахарной промышленности, для дубления кожи и для производства отбеливателя. При строительстве используется тестообразная смесь гашеной извести с цементом и песком.

Химические свойства гидроксида кальция
Гидроксид кальция, как и все основания, реагирует с кислотами:
Гидроксид кальция также способен образовывать соединения с углекислым газом. Раствор этого вещества на воздухе мутнеет, так как гидроксид кальция, как и другие сильные основания, реагирует с растворенной в воде углекислотой:
При нагревании до 400 градусов гидроксид кальция реагирует с окисью углерода:
Гидроксид кальция может реагировать с солями, в результате чего образуется осадок:
При температуре 520-580 градусов гидроксид кальция подвержен разложению. В результате образуются оксид кальция и вода:

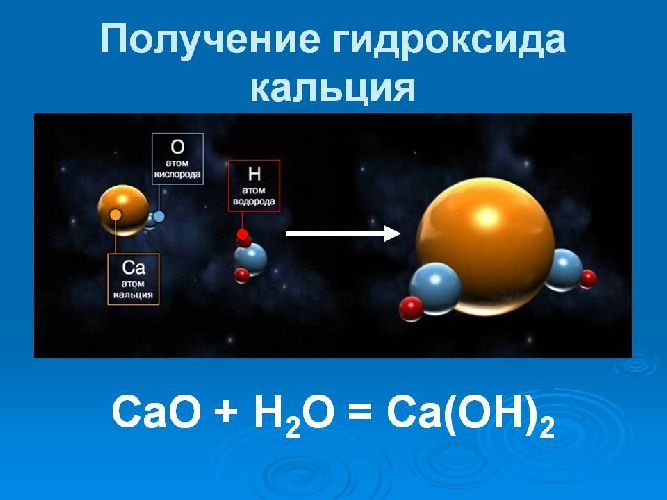
Получение гидроксида кальция происходит при химической реакции оксида кальция (негашеной извести) с водой. Этот процесс получил название «гашение извести». Уравнение реакции гашения извести выглядит следующим образом:
Что мы узнали?
Гидроксид кальция – сильное основание, легко растворимое в воде. Как и любой химический элемент, он обладает рядом свойств – способен вступать в реакцию с углекислым газом, солями, а также разлагается при высоких температурах. Гидроксид кальция применяется в строительстве и промышленности.








Комментирование закрыто