
Любое вещество в природе, в зависимости от внешней температуры и давления, может существовать в различных агрегатных состояниях. Одним из таких агрегатных состояний является твердое. Кратко рассмотрим особенности строения твердых тел.
Вещество, молекулы которого удерживаются на постоянном расстоянии друг от друга силами межмолекулярного притяжения, находится в твердом состоянии.
Кристаллические вещества
Чаще всего в твердом состоянии молекулы вещества расположены друг относительно друга не хаотично, а в строгом порядке, образуя ту или иную пространственную структуру. С молекулярной точки зрения, такая структура энергетически выгодна, в ней молекулы вещества имеют наименьшую потенциальную энергию.
Строгий порядок при этом определяет геометрическую форму вещества в этом состоянии. Такая геометрическая форма называется кристаллом.

Конкретная форма кристаллов может быть самой различной. Например, кристалл поваренной соли имеет форму куба. Если взять соль крупного помола, и рассмотреть ее через лупу, можно убедиться, что углы между гранями кристаллов всегда прямые.
Кристалл льда имеет ажурную шестигранную структуру: модель ледяного кристалла достаточно сложна, но ее шесть граней можно видеть в снежинках.
Кристалл графита имеет слоистую структуру. Именно это позволяет карандашу рисовать: на бумаге остаются слои кристалла графита.
Пространственная организация кристаллов нередко определяет такое важное свойство, как анизотропия — различие физических свойств кристалла в зависимости от направления.
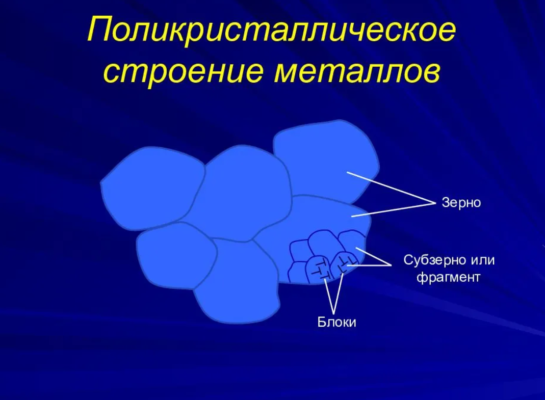
Наконец, еще одним важным свойством кристаллического вещества является возможность поликристаллизации. В этом случае отдельные кристаллы вещества оказываются хаотично соединены силами межмолекулярного притяжения, иногда даже «врастая» друг в друга. Наиболее часто такое свойство демонстрируют металлы. Если поглядеть через лупу на кромку излома хрупкого чугуна, можно легко увидеть его поликристаллическое строение.
Аморфные вещества
Существует также класс аморфных веществ, молекулы которых никогда не образуют строгих пространственных структур и всегда располагаются хаотично. Такие вещества нередко рассматриваются как жидкости с крайне высокой вязкостью. К аморфным веществам относятся смолы, пластмассы, стекло.
Битум в твердом состоянии похож на кристалл. Он не меняет формы, растрескивается при ударах, имеет твердость выше, чем у графита. Однако эксперимент, начатый в Квинслендском университете в 1927 г, и продолжающийся до сих пор, показал, что битум может очень медленно течь через воронку под действием тяжести. К настоящему времени из воронки упало девять капель. Подсчитано, что вязкость битума примерно в $2.3×10^{11}$ раз больше, чем у воды.

Что мы узнали?
Строение твердых тел может быть кристаллическим или аморфным. В кристалле молекулы занимают строго определенное пространственное положение. В результате кристалл имеет определенную геометрическую форму, а также ему свойственна анизотропия. Аморфные вещества подобны жидкостям с очень высокой вязкостью.








Комментирование закрыто